Der menschliche Körper kann sich selbst heilen – jedoch nur begrenzt. Die regenerative Medizin setzt genau hier an und versucht, mit Stammzellen, innovativen Materialien und neuen Therapien die Selbstheilung gezielt zu unterstützen. Wir werfen einen Blick auf aktuelle Forschungen und vielversprechende Ansätze.
Ein Gedanke, ein Schritt, ein Atemzug – vieles, was für uns selbstverständlich ist, basiert auf hochkomplexen biologischen Prozessen. Im menschlichen Körper arbeiten Milliarden von Zellen, Signalen und Strukturen präzise zusammen und ermöglichen so Bewegung, Wahrnehmung und Leben.
Gleichzeitig verfügt der Körper über die Fähigkeit, sich selbst zu reparieren. Wunden schließen sich, Knochen wachsen zusammen, Gewebe erneuert sich. Diese Prozesse laufen meist unbemerkt ab und sorgen dafür, dass Funktionen aufrechterhalten werden.
Doch diese Selbstheilungskräfte sind nicht unbegrenzt. In manchen Fällen reichen sie nicht aus, um Schäden vollständig auszugleichen oder langfristig zu verhindern. Genau hier setzt die Forschung an: Sie versucht zu verstehen, wie sich diese natürlichen Reparaturmechanismen gezielt unterstützen, verstärken oder neu anstoßen lassen.
Ziel ist es, Therapien zu entwickeln, die den Körper nicht ersetzen, sondern ihm helfen, sich selbst zu regenerieren. Dabei kommen unterschiedliche Ansätze zum Einsatz – von biologischen Prozessen bis hin zu neuartigen Materialien, die Heilungsprozesse aktiv fördern. Auch in Regensburg arbeiten Forschende aus Medizin, Biologie und Materialwissenschaft gemeinsam an der Frage, wie sich diese Potenziale künftig besser nutzen lassen.
Eine dieser Forscherinnen ist Prof. Dr. Susanne Grässel. Sie leitet die Abteilung für Experimentelle Orthopädie an der Orthopädischen Klinik der Universität Regensburg und forscht am Zentrum für medizinische Biotechnologie im BioPark. Dort beschäftigt sie sich seit vielen Jahren mit Erkrankungen des Bewegungsapparates, insbesondere mit Arthrose – einer Krankheit, von der weltweit rund 600 Millionen Menschen betroffen sind und die nach und nach die Gelenksknorpel und andere Gewebe zerstört und progressiv schwere Gelenkschäden verursacht.

Prof. Dr. Susanne Grässel, Orthopädische Klinik für die Universität Regensburg, Abteilung Experimentelle Orthopädie. © Prof. Dr. Susanne Grässel
Wenn der Knorpel seine Schutzfunktion verliert
In gesundem Zustand fungieren Knorpel als stoßdämpfende Gleitschicht zwischen den Knochen und sorgen für reibungslose und schmerzfreie Bewegungen. Dieses glatte, weiße Gewebe besteht zu 70 bis 80 Prozent aus Wasser. Der Rest setzt sich aus Kollagenfasern, Knorpelzellen und großen Molekülkomplexen, den sogenannten Proteoglykanen, zusammen. Diese wirken wie winzige Schwämme: Sie binden Wasser und halten es im Gewebe fest. Gemeinsam mit der Gelenkflüssigkeit, entsteht so eine Art elastisches „Wasserkissen“. Wird das Gelenk belastet, wird dieses Wasser kurzzeitig herausgedrückt und anschließend wieder aufgenommen.
Genau dieses Zusammenspiel verleiht dem Knorpel seine besondere Eigenschaft: Er ist gleichzeitig stabil und elastisch – fest genug, um Belastungen standzuhalten und flexibel genug, um Stöße abzufedern.
Tritt eine Arthrose ein, beginnen die Knorpel zu degenerieren. Ihre Oberflächen fransen aus, werden spröde und verlieren an Elastizität. Es entstehen Risse, die bis zum darunterliegenden Knochen reichen können. Gleichzeitig verändert sich auch dieser: Zunächst wird er poröser, es können schmerzhafte Zysten entstehen, später verdichtet er sich krankhaft. Arthrose ist daher keine reine Knorpelerkrankung – ein Punkt, den auch Prof. Dr. Grässel betont: „Ein Gelenk besteht aus vielen unterschiedlichen Geweben, und letztlich sind sie alle betroffen, nicht nur der Knorpel.“
Arthrose: Eine Erkrankung mit vielen Ursachen
Eine der größten Herausforderungen ist der schleichende Verlauf. Die Knorpelabnutzung beginnt oft bereits 20 oder 30 Jahre vor der Diagnose. Da Knorpel keine Nerven enthalten, merken die Betroffenen jedoch nichts davon. „Das Problem ist grundsätzlich, dass die Frühstadien oft unbemerkt bleiben, weil Patientinnen und Patienten meist erst dann zum Arzt gehen, wenn Schmerzen auftreten“, so die Professorin. „Dann ist die Erkrankung häufig bereits in einem Stadium, in dem eine Heilung nicht mehr möglich ist.“
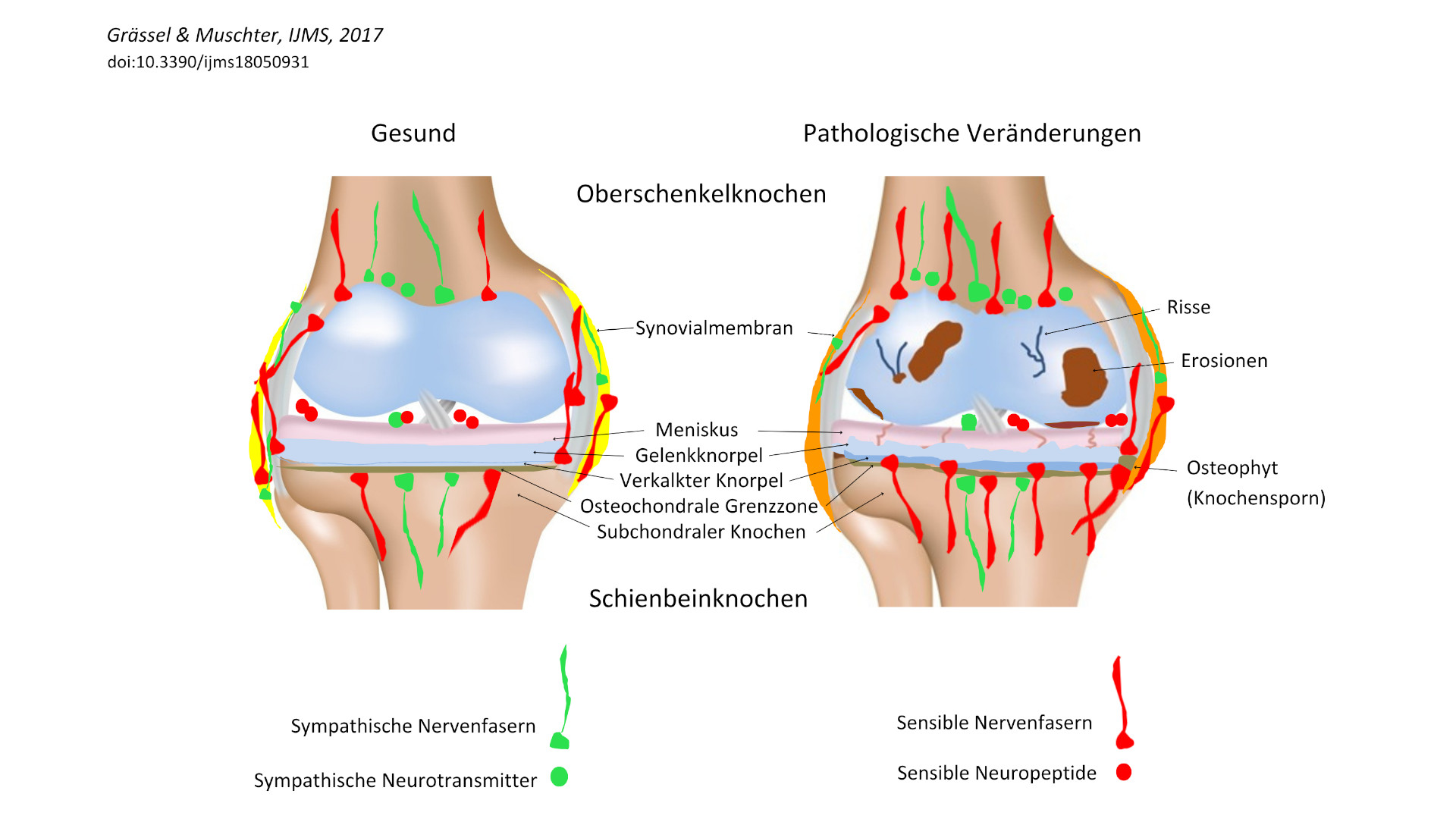
Gesundes (links) vs. arthrotisch verändertes Kniegelenk (rechts) mit Darstellung sympathischer (grün) und sensibler (rot) Nervenversorgung. © Grässel & Muschter, UMS, 2017
Theoretisch ließen sich Veränderungen mit bildgebenden Verfahren wie dem MRT frühzeitig erkennen. In der Praxis lässt sich das jedoch kaum umsetzen. Zum einen werden solche Untersuchungen ohne Beschwerden von den Krankenkassen in der Regel nicht bezahlt. Zum anderen stellt sich die Frage, welches Gelenk überhaupt untersucht werden sollte, denn Arthrose kann nahezu überall im Körper auftreten: in Knie und Hüfte ebenso wie in den Fingern, an der Wirbelsäule oder am Sprunggelenk.
Im Alltag wird Arthrose häufig als reine Abnutzung verstanden, denn Knorpel müssen hohen Belastungen standhalten. Tatsächlich wirken jedoch zahlreiche Faktoren zusammen. Neben mechanischer Belastung – etwa durch Übergewicht, Fehlstellungen der Beine oder Extremsport – spielen auch genetische Veranlagung, Stoffwechselerkrankungen wie Diabetes, frühere Verletzungen oder hormonelle Veränderungen eine Rolle.
Entzündung und Schmerz: Ein komplexes Zusammenspiel
Hinzu kommt ein entscheidender Faktor, der lange unterschätzt wurde: Entzündung. Anders als bei der rheumatoiden Arthritis handelt es sich bei Arthrose um eine niedrigschwellige, aber dauerhafte Entzündungsaktivität. Versuche, Medikamente aus der Rheumatherapie zu übertragen, sind bislang gescheitert. Ein Grund dafür ist, dass bei Arthrose nicht einzelne Entzündungsfaktoren vorliegen, sondern viele verschiedene gleichzeitig wirken. Dies macht deutlich, warum sich Arthrose so schwer behandeln lässt. Selbst wenn es gelänge, Knorpelgewebe neu zu bilden, würden die zugrunde liegenden Entzündungen weiterhin bestehen und den Regenerationsprozess stören. Für die Forschung bedeutet das: Es reicht nicht aus, einzelne Aspekte der Erkrankung zu behandeln – vielmehr müssen mehrere Prozesse gleichzeitig beeinflusst werden.
Genau hier setzt die Forschung von Prof. Dr. Grässel an. Ihre Arbeitsgruppe untersucht die Rolle des Nervensystems im Gelenk. Dabei geht es nicht nur um Schmerz, sondern auch um Botenstoffe, die von Nerven freigesetzt werden und Entzündungsprozesse beeinflussen. Vereinfacht gesagt, kann das sensible nociceptive Nervensystem, das für die Erkennung, Weiterleitung und Verarbeitung von potenziell oder tatsächlich gewebeschädigenden Reizen zuständig ist, Entzündungen verstärken und zugleich die Schmerzempfindung erhöhen – es wirkt also aktiv am Krankheitsverlauf mit.
Entscheidend ist jedoch: Schmerz entsteht nicht allein durch das Ausmaß des Gewebeschadens, sondern durch ein Zusammenspiel aus Entzündung, dem Nervensystem und der Art, wie der Körper auf Reize aus dem betroffenen Gewebe reagiert. Das kann von Mensch zu Mensch variieren. Diese Zusammenhänge können erklären, warum strukturelle Schäden und Schmerzen nicht immer parallel verlaufen. Manche Menschen haben starke Beschwerden bei vergleichsweise geringen Veränderungen, andere bemerken lange Zeit kaum etwas, obwohl das Gelenk bereits stark geschädigt ist.
Neue Ansätze: Stammzellen und regenerative Prozesse
Genau diese Komplexität zeigt, warum neue Therapieansätze notwendig sind, die mehrere Krankheitsprozesse gleichzeitig beeinflussen.
Eine wichtige Rolle spielen dabei Stammzellen. Sie gelten als vielversprechend, weil sie nicht nur das Potenzial haben, sich in unterschiedliche Zelltypen zu entwickeln, sondern auch sogenannte extrazelluläre Vesikel freisetzen. Diese kleinen Partikel enthalten verschiedene Botenstoffe, die im Gelenk regenerative Prozesse anstoßen und Entzündungen beeinflussen können.
„Meine Hoffnung wäre, dass man eines Tages einen ‚Cocktail’ aus verschiedenen Faktoren entwickeln kann, der direkt ins Gelenk injiziert werden kann“, so Prof. Dr. Grässel. „Ein solcher Cocktail müsste mehrere Dinge gleichzeitig bewirken: die Entzündung reduzieren und die Regeneration der Gewebe fördern.“
Noch stehen diese Ansätze am Anfang. Ein zentrales Problem bleibt die Komplexität der Erkrankung. Arthrose verläuft bei jedem Menschen unterschiedlich: Bei manchen steht der Knorpelschaden im Vordergrund, bei anderen die Entzündung oder die Veränderungen im Knochen. Eine einheitliche Therapie für alle Patientinnen und Patienten kann diesen Unterschieden nicht gerecht werden.
Materialien, die heilen helfen
Während ein Teil der Forschung versucht, über biologische Prozesse wie Stammzellen und Botenstoffe das Krankheitsgeschehen zu beeinflussen, verfolgt ein weiterer Ansatz einen grundlegend anderen Weg: Statt den Körper ausschließlich von innen heraus zur Regeneration anzuregen, sollen Materialien gezielt dabei helfen, geschädigte Strukturen zu stabilisieren und Heilungsprozesse zu unterstützen.
Mit genau dieser Frage beschäftigt sich Prof. Dr. Helga Hornberger, Professorin für Biomaterialien und Materialwissenschaft an der Fakultät Maschinenbau der OTH Regensburg. Sie forscht im Bereich der Biomaterialien und untersucht, wie sich künstliche Materialien so entwickeln lassen, dass sie nicht nur verträglich sind, sondern auch aktiv mit dem Körper zusammenarbeiten.
„In der regenerativen Medizin geht es längst nicht mehr nur darum, dass ein Implantatmaterial nicht schadet, sondern vielmehr darum, dass es Prozesse im Gewebe unterstützt – etwa indem es Zellwachstum fördert oder als Leitstruktur für neue Gewebe dient“, so die Professorin.

Prof. Dr. Helga Hornberger, Professorin für Biomaterialien, Materialwissenschaft Fakultät Maschinenbau. © OTH Regensburg
Ein besonders vielversprechender Ansatz sind sogenannte Hydrogele. Dabei handelt es sich um wasserhaltige Polymernetzwerke, deren Eigenschaften denen von bestimmtem körpereigenem Gewebe erstaunlich ähnlich sind. Die Idee: Ein zunächst flüssiges Material wird in geschädigtes Knorpelgewebe eingebracht und verdickt sich dort innerhalb weniger Minuten zu einem Gel. So entsteht im Gewebe eine Art Gerüst, das sich mit Wasser anreichert. Ähnlich wie gesunder Knorpel kann dieses Gel Druck aufnehmen und wieder abgeben – eine wichtige Voraussetzung für die Dämpfungsfunktion im Gelenk. Ziel sei es, so Hornberger, „die verlorengegangenen Dämpfungseigenschaften wiederherzustellen“.
Noch befindet sich dieser Ansatz in der Forschung. Eine der großen Herausforderungen besteht darin, Materialien zu entwickeln, die im Körper zuverlässig reagieren, gut verträglich sind und sich optimal in das bestehende Gewebe integrieren. „Der Körper verträgt nicht jedes Hydrogel gleich gut“, sagt Hornberger. Deshalb müsse man genau verstehen, „wie diese Materialien mit dem Gewebe wechselwirken“ und wie sich ihre Eigenschaften gezielt steuern lassen.
Doch nicht in allen Fällen geht es darum, weiches Gewebe wie Knorpel nachzuahmen oder aufzubauen. Gerade bei Knochenbrüchen braucht der Körper zunächst vor allem eines: Stabilität. Hier kommen andere Materialien ins Spiel – und damit ein weiterer Forschungsbereich von Prof. Dr. Helga Hornberger.

Durchführung von elektrochemischen Korrosionsmessungen zur Analyseder Materialbeständigkeit. © A. Ellmeier, OTH Regensburg
Magnesium: Implantate auf Zeit
Neben Hydrogelen beschäftigt sie sich mit sogenannten resorbierbaren Metallen, insbesondere mit Magnesium. Diese Materialien sollen eine Aufgabe erfüllen, die klassische Implantate bis heute nur teilweise leisten können: Sie stabilisieren den Körper – und lösen sich anschließend auf.
Bisher werden bei Knochenbrüchen häufig Schrauben, Platten oder Nägel aus Titan oder Stahl eingesetzt. Sie sind gut verträglich und belastbar, bleiben jedoch entweder dauerhaft im Körper zurück oder müssen in einer zweiten Operation entfernt werden. Ein resorbierbares Implantat jedoch würde den Knochen so lange stabilisieren, bis er verheilt ist – und anschließend vom Körper nach und nach abgebaut werden. Eine zweite Operation wäre damit nicht mehr notwendig. Das würde nicht nur das Risiko von Komplikationen und Infektionen senken, sondern auch die psychische und körperliche Belastung für Patientinnen und Patienten deutlich reduzieren.
Magnesium bietet dafür die idealen Voraussetzungen. Anders als viele andere Metalle ist es gut verträglich und wird im Körper zu Ionen abgebaut. „Magnesium ist etwas, das der Körper für viele physiologische Prozesse ohnehin braucht. Daher nehmen viele Menschen Magnesiumpräparate zur Nahrungsergänzung ein“, so die Materialwissenschaftlerin.
Die Herausforderung liegt jedoch im Detail. Der Abbauprozess muss exakt gesteuert werden. „Es geht darum, dass sich das Material weder zu schnell noch zu langsam zersetzt“, sagt Hornberger. „Korrodiert das Implantat inhomogen, könnte irgendwo ein Loch entstehen, während andere Stellen noch fast intakt sind. Dadurch könnte das Implantat an einer Stelle zusammenbrechen und seine mechanische Stabilität nicht lange genug aufrechterhalten“, erklärt die Professorin.
Daher arbeitet ihre Forschungsgruppe unter anderem an speziellen Oberflächenbehandlungen wie der Elektropolitur, die das Korrosionsverhalten gezielt beeinflussen sollen. „Dabei handelt es sich um ein elektrochemisches Verfahren, bei dem die Oberfläche Ion für Ion abgetragen wird. So bekommt man spiegelnde, sehr glatte Oberflächen ohne Defekte. Das ist praktisch, weil man ganze Bauteile von allen Seiten bearbeiten kann, ohne sie mechanisch schleifen zu müssen“, erklärt Prof. Dr. Hornberger. Für diese Arbeiten – insbesondere die Entwicklung eigener Elektrolyte und die gezielte Untersuchung des Korrosionsverhaltens – wurde die Promovendin aus ihrer Forschungsgruppe im vergangenen Jahr mit dem BioPark-Preis ausgezeichnet.
Erste Anwendungen zeigen, dass dieser Ansatz bereits funktioniert. Vor allem bei kleineren Implantaten, etwa in der Handchirurgie, kommen zunehmend Magnesiumschrauben zum Einsatz. Auch in anderen Bereichen, etwa bei Gefäßstützen, sogenannten Stents, wird an abbaubaren Varianten geforscht.
Für die regenerative Medizin eröffnet sich damit eine neue Perspektive: Materialien, die nicht nur passiv im Körper verbleiben, sondern aktiv am Heilungsprozess teilnehmen – und danach wieder verschwinden. Hornberger beschreibt diese Idee als eine Art Zusammenarbeit zwischen Material und Körper: Strukturen würden geschaffen, die den Heilungsprozess unterstützen, bis der Körper sie selbst ersetzen kann.
Bioaktives Glas: Vom Fremdkörper zum Helfer
Ein weiterer Ansatz zeigt, wie weit sich diese Idee bereits in der Praxis umsetzen lässt. Priv. Doz. Dr. med. Fabian Westhauser – Leitender Oberarzt und Facharzt für Orthopädie und Unfallchirurgie sowie für spezielle orthopädische Chirurgie am Asklepios Klinikum in Bad Abbach – verbindet klinische Arbeit und Forschung. Er arbeitet mit einem Material, das den meisten eher aus dem Alltag bekannt ist: Glas. Genauer gesagt handelt es sich um sogenanntes bioaktives Glas, das im Körper eine erstaunliche Eigenschaft entwickelt – es wird nicht nur angenommen, sondern auch aktiv in Heilungsprozesse eingebunden.
Die Idee, Glas in der Chirurgie einzusetzen, wirkt auf den ersten Blick ungewöhnlich – tatsächlich reicht sie aber weiter zurück, als man vermuten würde. Während des Vietnamkriegs verloren viele schwer verletzte Soldaten ihre Gliedmaßen, weil die bei Operationen verwendeten Materialien vom Körper abgestoßen wurden. Nach einem zufälligen Austausch des Materialwissenschaftlers Larry Hench aus den USA mit einem Militärarzt erhielt Hench den Auftrag, ein Material für Knochenverletzungen zu entwickeln, das vom Körper toleriert würde. Damit wurde der Grundstein für den Einsatz von bioaktivem Glas in der Medizin gelegt.
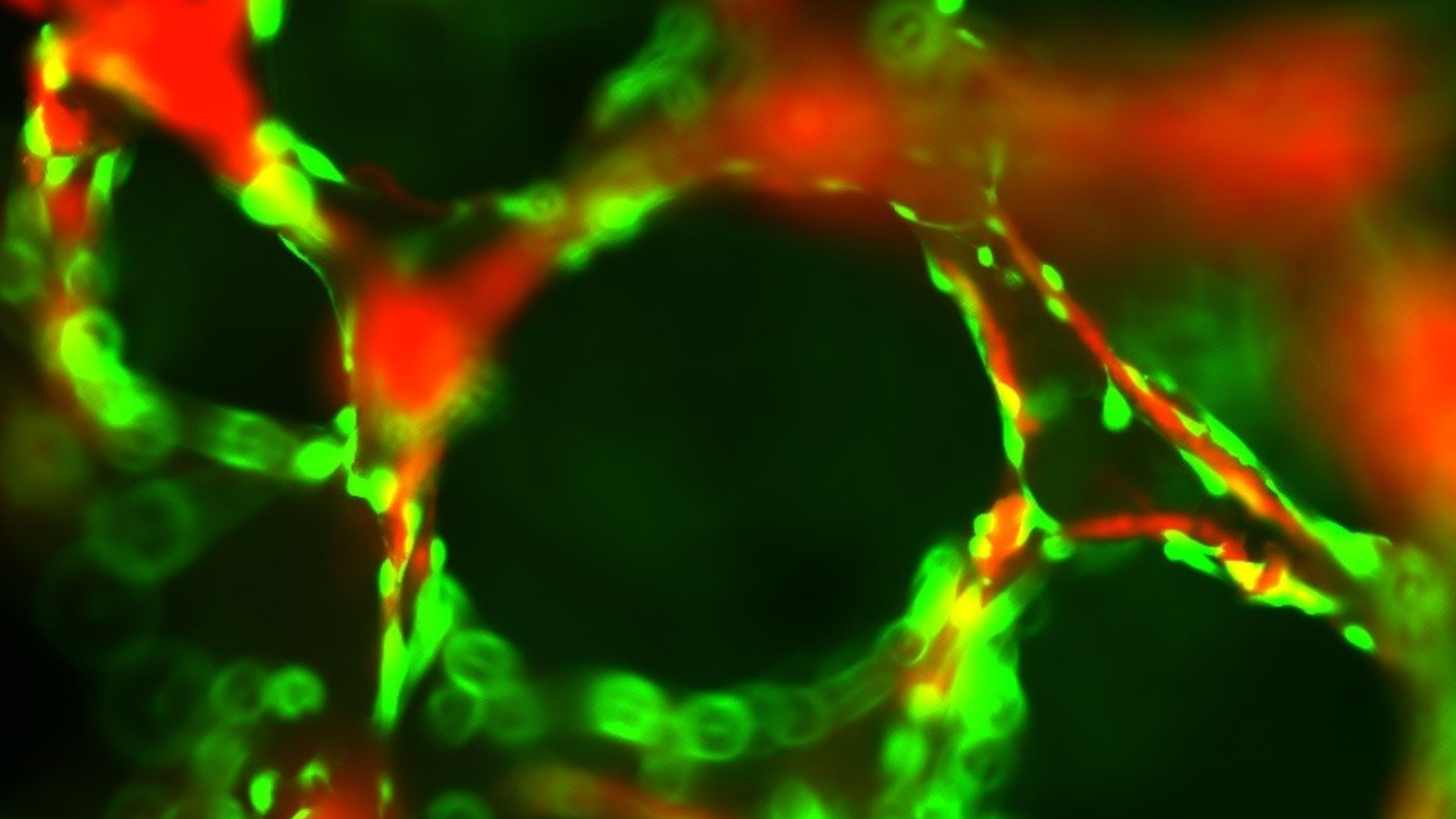
Dreidimensionale Glasbausteine (rot), bewachsen von Zellen (grün), veranschaulichen die stimulierende Wirkung von Glas auf das Zellwachstum. © Andreas Scheurle
Dass ausgerechnet dieses spröde und zerbrechliche Material dafür infrage kommen könnte, erscheint zunächst widersprüchlich. Doch bioaktives Glas unterscheidet sich grundlegend von Alltagsglas. Vereinfacht gesagt, bewegt es sich chemisch zwischen festem Stoff und Flüssigkeit – eine Struktur, die es reaktiver macht. Genau diese Eigenschaft ermöglicht es, mit dem Körper in Wechselwirkung zu treten und Heilungsprozesse aktiv zu unterstützen.
Wird das Material in den Körper eingebracht, beginnt seine Oberfläche mit der Umgebung zu reagieren. Bestandteile des Glases lösen sich, werden durch körpereigene Stoffe ersetzt und führen dazu, dass sich auf der Oberfläche eine Substanz bildet, die dem natürlichen Knochen sehr ähnlich ist. „Das Entscheidende ist, dass das Material eine chemische Bindung zum Knochen eingeht“, erklärt Dr. Westhauser. „Dadurch wird es vom Körper nicht als fremd erkannt, sondern in das Gewebe integriert. Ferner stimulieren die aus dem Glas freigesetzten Bestandteile den Stoffwechsel der umgebenden Knochenzellen dazu, neuen Knochen aufzubauen.“
Im Gegensatz zu Knochenzement, der lediglich Hohlräume auffüllt, verfolgt bioaktives Glas ein anderes Prinzip: Es dient als temporäres Gerüst. „Das Glas wird vollständig abgebaut – und im gleichen Zeitraum bildet der Körper neues Knochengewebe“, beschreibt Dr. Westhauser den Prozess. Ziel ist eine möglichst vollständige Regeneration, bei der am Ende kein Fremdmaterial zurückbleibt.
Besonders bemerkenswert ist dabei, dass das Material nicht nur den Knochenaufbau unterstützt, sondern auch antibakterielle Eigenschaften aufweist. Gerade bei komplizierten Eingriffen oder Infektionen leistet Glas hier einen zusätzlichen und möglicherweise entscheidenden Beitrag zur schnelleren Genesung.
Anders als viele experimentelle Ansätze ist bioaktives Glas bereits im klinischen Alltag angekommen. Es wird eingesetzt, um Knochendefekte zu behandeln – etwa bei Schäden, die durch ausgelockerte Gelenkimplantate verursacht wurden oder nach der Entfernung von gutartigen Knochentumoren – und dient dabei als Gerüst, auf dem neues Knochengewebe entstehen kann.
Besonders deutlich wird das am Beispiel des sogenannten Riesenzelltumors. Diese Tumoren zerstören den Knochen von innen. Nach der Operation bleibt oft ein Hohlraum zurück, den der Körper allein nicht mehr schließen kann. Bisher wurde er meist mit Knochenzement gefüllt: ein Material, das stabilisiert, aber im Körper verbleibt und sich nicht in lebendes Gewebe verwandelt.
Bioaktives Glas füllt diesen Hohlraum jedoch nicht nur, sondern wird nach und nach vom Körper umgebaut. Während sich das Material auflöst, wächst neues Knochengewebe nach. Im Labor machte Dr. Westhauser eine weitere höchst interessante Entdeckung: „Wir sehen, dass Tumorzellen im Kontakt mit Glas absterben, während gesunde Knochenzellen davon profitieren“, so der Arzt. Warum das so ist, wird derzeit noch erforscht.
Für die Medizin eröffnet das jedoch möglicherweise neue Perspektiven und Behandlungsansätze.
Die Erfahrungen aus der Praxis überzeugen. „Es vergeht keine Woche, in der ich kein Glas einsetze“, so Dr. Westhauser. Gleichzeitig zeigt dieses Beispiel, wie komplex die Entwicklung neuer Therapien ist. Obwohl bioaktives Glas bereits seit Jahrzehnten bekannt ist, wird bis heute daran geforscht, die zugrunde liegenden biologischen Mechanismen vollständig zu verstehen. Fortschritt in der regenerativen Medizin bedeutet deshalb oft nicht nur, neue Materialien zu entwickeln, sondern vorhandene besser zu verstehen und gezielter einzusetzen.
Damit schließt sich der Kreis: Ob über Zellen, über Botenstoffe oder über Materialien – alle Ansätze verfolgen letztlich dasselbe Ziel. Sie wollen den Körper nicht ersetzen, sondern ihn dabei unterstützen, sich selbst zu reparieren. Die regenerative Medizin steht dabei noch am Anfang. Doch die Vielfalt der Ansätze zeigt, wie groß das Potenzial ist, Krankheiten künftig nicht nur zu behandeln, sondern Heilungsprozesse aktiv zu steuern.
Was wir selbst für unsere Gesundheit tun können
Auch wenn die Forschung schon weit fortgeschritten ist, bleibt ein großer Teil unserer Gesundheit in unserer eigenen Verantwortung. Denn viele Prozesse im Körper lassen sich zwar medizinisch beeinflussen, doch ihr Verlauf wird auch durch den Alltag geprägt.
Bewegung spielt dabei eine zentrale Rolle. Gelenke werden nicht direkt über Blutgefäße versorgt, sondern über die Gelenkflüssigkeit. Diese wird durch einen Pumpmechanismus im Gewebe verteilt – und der funktioniert nur, wenn das Gelenk regelmäßig bewegt wird. Entscheidend ist dabei das richtige Maß: Zu wenig Bewegung schadet ebenso wie Überlastung.
Auch die Ernährung hat Einfluss. Besonders Bauchfett gilt als stoffwechselaktiv und fördert Entzündungsprozesse im Körper, die sich auch auf die Gelenke auswirken können. Eine ausgewogene Ernährung, regelmäßige Bewegung, möglichst wenig Alkohol und der Verzicht auf Rauchen können dazu beitragen, diese Prozesse zu reduzieren.
Ebenso wichtig ist es, Verletzungen ernst zu nehmen. Unbehandelte Schäden an Knorpeln oder Bändern können Jahre später zu Problemen führen – oft, ohne dass ein direkter Zusammenhang noch erkennbar ist.
Die Medizin kann heute viel leisten – von konservativen Therapien bis hin zu modernen Implantaten, die Beweglichkeit und Lebensqualität zurückgeben. Doch sie kann die natürlichen Funktionen des Körpers nicht ersetzen.
Am Ende zeigt sich: Die Forschung eröffnet neue Möglichkeiten, den Körper bei der Heilung zu unterstützen. Wie gut diese Möglichkeiten wirken, hängt jedoch auch davon ab, wie wir selbst mit ihm umgehen.
Ein Bericht von Kathrin Gnilka I filter Magazin